發布時間:2016-05-24閱讀次數: 894

早在1000年以前,阿拉伯醫生Abulcasis(1013-1017)就發明了活檢技術。活檢的好處是醫生可以根據病灶組織學結構對病情做出判斷。隨著近幾年測序技術的發展,醫生可以對患者組織測序進而給出更加精確的診斷結果。
但隨著對腫瘤研究的深入,科學家發現在癌癥的診斷和治療過程中組織活檢技術有一定的局限性。主要表現為:腫瘤具有異質性,對于癌細胞已經發生轉移的患者而言,僅僅取某個部位的腫瘤組織,并不能反映患者的整體情況,但對所有的腫瘤組織都取樣檢測又不切實際;某些患者自身的情況決定了他不適合做組織活檢;受到手術的擾動之后,有些腫瘤有加速轉移的風險;組織活檢的滯后性對患者的治療也是不利的。因此對于癌癥的診斷和檢測技術有更高的要求。
液體活檢技術的出現,解決了上述的問題,也提前了癌癥的診斷時間。這也是液體活檢技術被《麻省理工大學科技評論》評選為“2015年十大突破技術”的原因。
作為體外診斷的一個分支,液體活檢就是通過血液或者尿液等對癌癥等疾病做出診斷。其優勢在于能通過非侵入性取樣降低活檢的危害,而且有效延長患者生存期,性價比高。目前液體活檢的主要檢測物包括檢測血液中游離的循環腫瘤細胞(CTCs),循環腫瘤DNA(ctDNA)碎片,循環RNA(Circulating RNA)和外泌體(攜帶有細胞來源相關的多種蛋白質,脂類,DNA,RNA等)。其中,ctDNA,RNA和外泌體是腫瘤細胞自身分泌或死亡時釋放的物質。
下面我們對液體活檢檢測物及研究進展做簡要的介紹。
液體活檢主要檢測物
循環腫瘤細胞(Circulating Tumor Cells,CTCs)
1869年,澳大利亞籍醫生Ashworth首次提出循環腫瘤細胞(Circulating Tumor Cells,CTCs)的概念。1976年,Nowell將CTCs的定義修正為來源于原發腫瘤或轉移腫瘤,獲得脫離基底膜的能力并通過組織基質進入血管的腫瘤細胞。目前,CTCs是指存在于外周血中的各類腫瘤細胞的統稱。CTCs以不同形態存在于外周血中,既有游離的單個CTCs,也有聚集成團的細胞團(CTM,Circulating Tumor Microemboli),腫瘤細胞在進入外周血循環的過程中會發生上皮-間質轉變(Epithelial Mesenchymal Transition,EMT)。
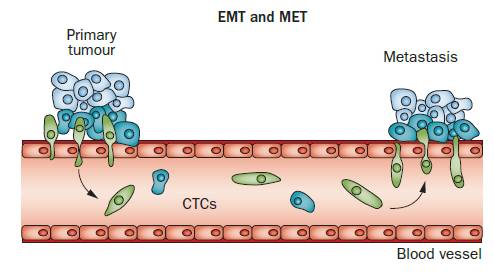
CTCs轉移過程中必經階段:
CTCs通過從腫瘤組織中脫落游走至血管,穿過血管進入血循環,克服自身及血循環中各種因素的殺傷作用,到最后定植形成新的轉移灶等多個生理步驟,使得CTCs可順利侵襲轉移從而促進相關疾病的進展。
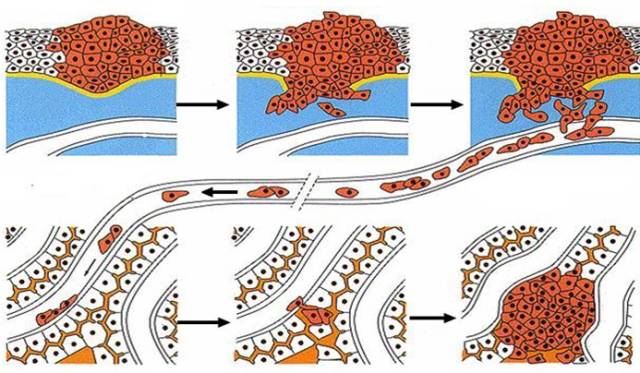
CTCs的檢測:
對CTCs檢測包含細胞富集和細胞檢測兩部分,可以進行不同的組合,形成不同的技術。最常見的富集方法是抗體介導或物理方法富集,接下來進行免疫組織化學計數或遺傳分析。

A行顯示了磁珠-抗體富集方法;B行顯示了物理富集方法;C行顯示了最常用的細胞檢測方法。
血漿游離腫瘤DNA('Cell-Free' Circulating Tumor DNA,ctDNA
ctDNA(circulating tumor DNA)即循環腫瘤DNA是人體血液循環系統中不斷流動的攜帶一定特征(包括突變,缺少,插入,重排,拷貝數異常,甲基化等)來自腫瘤基因的DNA片段。一般來源于壞死或凋亡的腫瘤細胞,循環腫瘤細胞和腫瘤細胞分泌的外排體,但是在了解ctDNA之前,我們要知道另一個與之相關的概念—cfDNA。
cfDNA(cell-free DNA),或者叫血漿游離DNA,是血漿中游離存在的DNA,它們有的來自于正常細胞,有的來自于異常細胞(如腫瘤細胞),還有部分來自于我們外部(如病毒DNA)。
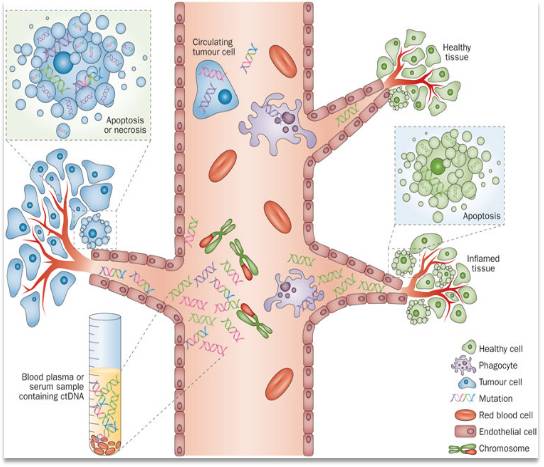
ctDNA的檢測:
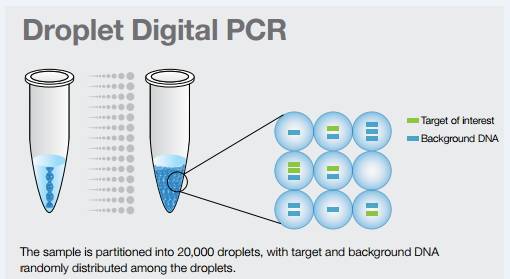
數字PCR
將一個標準PCR反應分配到大量微小的反應器中,在每個反應器中包含或不包含一個或多個拷貝的目標分子( DNA模板),實現“單分子模板PCR擴增”,擴增結束后,通過陽性反應器的數目“數出”目標序列的拷貝數。
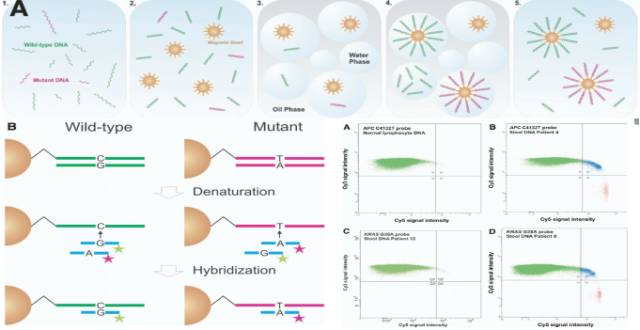
BEAMing技術
結合數字PCR與流式技術,利用特異性PCR引物擴增目標突變區后,與磁珠(磁珠上固定有特異的PCR引物)混合進行油包水單分子擴增反應。反乳化作用后,利用不同顏色的熒光探針結合磁珠上的PCR產物,發出紅色或綠色熒光,再利用流式細胞儀分析磁珠顏色來確定突變情況。
液體活檢的研究進展
液體活檢—治愈癌癥的可靠保障
近日,哈佛醫學院丹娜法伯癌癥研究院領導合作研究小組成功證實了液體活檢技術作為臨床工具識別特定病人的可行性。這種簡單液體活檢技術可快速且精準地檢測導致非小細胞肺癌(NSCLC)的兩種關鍵基因致病突變,進而幫助臨床醫生為病人制定針對上述兩種突變的化療藥單,提高非小細胞肺癌的臨床治療水平。“我們認為血漿基因分型在臨床測試中具有不可估量的應用潛力,這種癌癥常規基因印記的快速與無創篩查可以避免對傳統侵入性的活組織檢查的挑戰。”丹娜法伯/布列根女性醫院肺癌專家Geoffrey Oxnard博士說。(原文:Prospective Validation of Rapid Plasma Genotyping for the Detection of EGFR and KRAS Mutations in Advanced Lung Cancer)
Sci Transl Med:“液體活檢”可捕捉癌性突變
新國際著名雜志Science Translational Medicine在線刊登的一項新的研究報告中指出,一種新的基因測序技術可能比用傳統的腫瘤活檢技術檢測癌性突變更安全及廉價。這種叫做"TAm-Seq"的技術可通過收集血漿中循環DNA片段,放大與癌癥相關的DNA部分并深入挖掘基因序列來發現那些難以辨認的突變。Tim Forshew及其同事分析了來自一組晚期卵巢癌病人的腫瘤樣本并發現,有67%的病人帶有腫瘤抑制基因TP53的突變。
Cell:新型血檢技術或可擴大液體活檢的范圍
發表在Cell上的一篇報道中,華盛頓大學的科學家表示他們開發了一種新方法可以克服當前液體活檢技術的局限性,從而幫助鑒別哪些類型的細胞可以產生游離DNA;這種方法依賴于對個體機體中游離DNA的片段譜系的分析并將這種譜系信息同細胞多種死亡生理條件進行對比,可以擴大液體活檢的檢測范圍。
液體活檢技術使得癌癥早期階段的篩查成為可能,無論是腫瘤診斷,治療還是監控領域,液體活檢的優勢都使其成為最具發展潛力的腫瘤無創診斷手段,具有極高的臨床應用價值和市場前景。
相關會議推薦

2016液態活檢與臨床應用研討會
會議時間:2016.05.20-2016.05.21 會議地點:上海